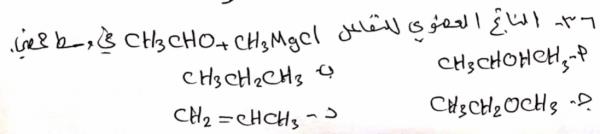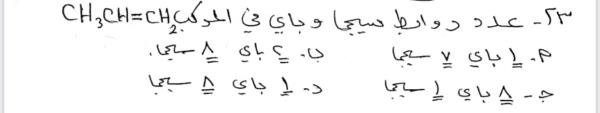امتحان الكيمياء للصف الثاني ثانوي | نماذج وأسئلة الفصل مراجعة 2025
يعد امتحان الكيمياء للصف الثاني ثانوي من أهم الامتحانات التي يتطلع الطلاب للنجاح فيها خلال الفصل مراجعة. نقدم لك في هذا المقال نماذج امتحانية محدثة وأسئلة متوقعة لتساعدك في التحضير بشكل فعّال، مع نصائح مهمة لاستكمال الاستعداد للامتحان بثقة. تابع القراءة لاكتشاف المزيد حول الأسئلة الأكثر شيوعاً وكيفية التفوق في امتحانك.
سؤال رقم 1
يعرف عدد التأكسد بأنه الشحنة الفعلية لأيون الذرة في المركبات الأيونية
الاجابات
نعم
لا
سؤال رقم 2
عند عمل خلية مكونة من قطب الهيدروجين المعياري وقطب القصدير Sn تحركت الالكترونات نحو قطب الهيدروجين وسجل الفولتميتر قراءة مقدارها 0,14 فولت . فإن جهد الاختزال للقصدير يساوي 0,14 فولت .
الاجابات
نعم
لا
سؤال رقم 3
إذا علمت أن +Ag أقوى كعامل مؤكسد من Cu+2 فإن الخلية الغلفانية المكونة من قطبي Ag/Cu تسري فيها الالكترونات عبر الاسلاك من قطب Ag نحو قطب Cu
الاجابات
نعم
لا
سؤال رقم 4
عدد تأكسد الكربون في سكر الغلوغوز C6H12O6 يساوي +4
الاجابات
نعم
لا
سؤال رقم 5
!ذا علمت أن Cd أقوى كعامل مختزل من Co , فإنه يمكن ترسيب أيونات الــ Co+2 من محاليل مركباته بواسطة الــ Cd .
الاجابات
نعم
لا
سؤال رقم 6
إذا علمت أن A+2 + 2e- → A له هE تساوي -0,40 فولت , فإنه لا يمكن حفظ محلول HCl المخفف في وعاء مصنوع من هذا العنصر .
الاجابات
نعم
لا
سؤال رقم 7
في التحول -HBrO → BrO3 مقدار التغير في عدد تأكسد البروم يساوي 6
الاجابات
نعم
لا
سؤال رقم 8
تحولات الطاقة في الخلية الغلفانية من كيميائية إلى كهربائية
الاجابات
نعم
لا
سؤال رقم 9
تحافظ القنطرة الملحية في الخلية الغلفانية على التوازن الكهربائي للخلية
الاجابات
نعم
لا
سؤال رقم 10
شحنة المصعد في الخلية الغلفانية موجبة
الاجابات
نعم
لا
سؤال رقم 11
في التفاعل :
Al + NO3- → AlO2- + NH3
العامل المؤكسد هو -NO3
الاجابات
نعم
لا
سؤال رقم 12
نصف التفاعل Cr+3 + 3e- → Cr يحتاج إلى عامل مؤكسد
الاجابات
نعم
لا
سؤال رقم 13
عدد تأكسد الكلور في المركب KClO3 يساوي +5
الاجابات
نعم
لا
سؤال رقم 14
العامل المختزل هو المادة التي تسبب أكسدة مادة أخرى
الاجابات
نعم
لا
سؤال رقم 15
اعتماداً على الجدول الذي يبين قيم جهود الاختزال المعيارية لعدد من الفلزات :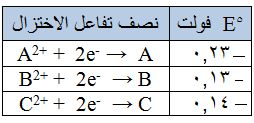

العبارة الصحيحة فيما يلي هي :
الاجابات
يمكن تحريك محلول يحتوي أيونات C+2 بمعلقة مصنوعة من الفلز A
الفلز B أقوى كعامل مختزل من الفلز A
تستطيع ذرات الفلز C ترسيب أيونات B+2
التفاعل A+2 + B → A + B+2 هو تفاعل تلقائي
سؤال رقم 16
اعتماداً على الجزء التالي من جدول جهود الاختزال المعيارية :
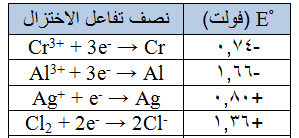

الفلز الأكثر ميلاً للتأكسد من الفلزات الواردة في الجدول هو :
الاجابات
Cl2
Al
Cr
Ag
سؤال رقم 17
لدى موازنة التفاعل التالي في وسط قاعدي :
CN- + MnO4- → CNO- + MnO2
فإن عدد مولات الالكترونات المفقودة أو المكتسبة في التفاعل يساوي:
الاجابات
2
4
6
3
سؤال رقم 18
العبارة الصحيحة والتي تصف قطب المهبط في الخلية الغلفانية هي :
الاجابات
يحدث عليه تفاعل اختزال وشحنته سالبة
شحنته موجبة وتزيد كتلته بمرور الزمن
يحدث عليه تفاعل تأكسد وشحنته سالبة
شحنته سالبة وتقل كتلته بمرور الزمن
سؤال رقم 19
يبين الجدول عدد من الخلايا الغلفانية ومعلومات عن كل منها :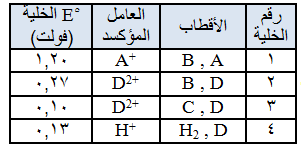

قيمة جهد الخلية التي أقطابها A/D يساوي :
الاجابات
0,80 فولت
0,40 فولت
0,67 فولت
0,93 فولت
سؤال رقم 20
في الجدول التالي :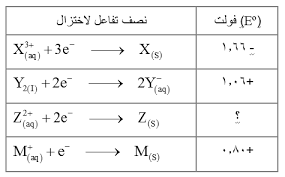

إذا علمت أن قيمة جهد الخلية المكونة من قطبي Z/X والتي يمثل فيها القطب X العامل المختزل يساوي 1,52 فولت ,فإن قيمة جهد الاختزال لنصف التفاعل
Z+2 +2e- → Z هو :
الاجابات
0,14 فولت
1,18 فولت
-0,14 فولت
-0,40 فولت
سؤال رقم 21
لدى دراسة الفلزات A , B , C والتي تكون أيونات ثنائية موجبة , وجد أن أيونات A+2 تستطيع أكسدة كل من ذرات B و C وأن ذرات العنصر B تستطيع ترسيب أيونات C+2 من محاليل أحد أملاحه . فإن ترتيبها حسب قوتها كعوامل مختزله هو :
الاجابات
A < C < B
C > A > B
B+2 < C+2 < A+2
B+2 > C+2 > A+2
سؤال رقم 22
لديك الجزء الأتي من جدول جهود الاختزال المعياربة :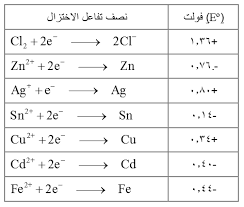

الفلزين اللذين يكونان خلية لها أقل جهد هما :
الاجابات
Cd/Sn
Ag/Cu
Fe/Cd
Fe/Zn
سؤال رقم 23
يمثل الشكل خلية غلفانية :
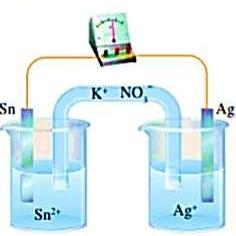

بناءاً على الشكل فإن :
الاجابات
قطب Sn هو المصعد وتزيد كتلته بمرور الزمن
يقل تركيز أيونات Sn+2 مع مرور الزمن في وعاء القطب Sn
قطب Ag هو المهبط وشحنته موجبة
تقل كتلة قطب Ag بمرور الزمن .
سؤال رقم 24
الجدول لعدد من الخلايا الغلفانية ومعلومات عنها :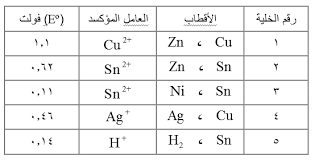

بناءأً على المعلومات الواردة في الجدول فإن العناصر التي تستطيع تجرير غاز الــ H2 من محاليل الحموض المخففة هي :
الاجابات
Cu , Ag
Ag , Sn
Sn , Zn , Ni
Cu , Ni
سؤال رقم 25
تم استخدام عدد من الفلزات والتي تكون جميعها أيونات ثنائية موجبة لعمل خلايا غلفانية كما في الجدول التالي :
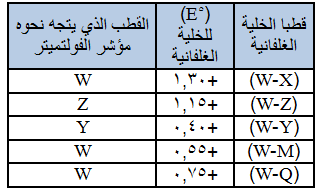

من المعلومات الواردة في الجدول فإن ترتيب هذه الفلزات حسب قوتها كعوامل مختزلة هو :
الاجابات
Z+2 < Y+2< W+2 < M+2< Q+2< X+2
Z > Y > W > M > Q > X
Z < Y < W < M < Q < X
Z < Y < W < X < Q < M
سؤال رقم 26
المعادلة النهائية الموزونة للتفاعل التالي والذي يحدث في وسط حمضي هي :
H2S + NO3- → S + NO
الاجابات
2H2S + 3NO3- → 2S + 3NO + 2H2O
3H2S + 2NO3- + 2H+ → 3S + 2NO + 4H2O
3H2S + 2NO3- + 2H2O → 3S + 2NO
3H2S + 2NO3- → 3S + 2NO + H2O
سؤال رقم 27

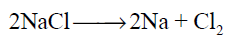
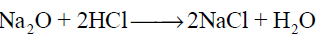
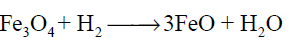
أحد التفاعلات التالية لا يعد تفاعل تأكسد واختزال :
الاجابات

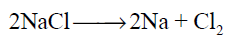
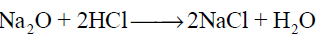
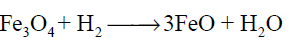
سؤال رقم 28
أعلى عدد تأكسد للنيتروجين ( N ) يكون في :
الاجابات
N2H4
NH3
-NO2
-NO3
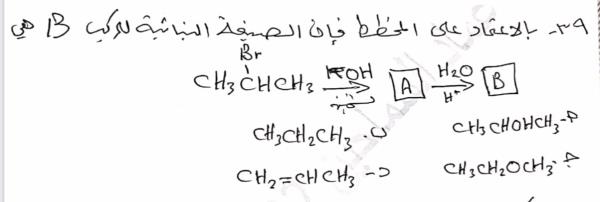
سؤال رقم 29
إذا علمت أن التفاعل التالي ممكن الحدوث في الظروف المعيارية :
-Br2 + Ni → Ni+2 + 2Br فإن العبارة الصحيحة فيما يلي هي :
الاجابات
Br2 عامل مختزل
Ni هو المهبط
-Br عامل مختزل أقوى من الــ Ni
Br2 عامل مؤكسد أقوى من الــ Ni+2
سؤال رقم 30
في التفاعل :
Cr2O7-2 + C2H6 O → Cr+3 + CO2
والذي يحدث في وسط حمضي . فإن المعادلة التي تمثل نصف تفاعل الاختزال الموزون هي :
الاجابات
-C2H6O + 3H2O → 2CO2 + 6H+ + 6e
-C2H6O + 3H2O → 2CO2 + 12H+ +12e
Cr2O7-2 + 14H+ + 6e- → 2Cr+3 + 7H2O
-Cr2O7-2 + 3H2O → 2Cr+3 +10H+ + 14e
سؤال رقم 31
أن تسلك المادة كعامل مؤكسد وكعامل مختزل في نفس التفاعل , تعبير عن :
الاجابات
العامل المؤكسد
التأكسد
التأكسد والاختزال الذاتي
الاختزال
سؤال رقم 32
أحد الآتية يمكن أن يسلك كعامل مؤكسد :
الاجابات
Na
+H
Ca
-H
سؤال رقم 33
في التفاعل :
Cr2O7-2 + C2H6O → Cr+3 + C2H4O
الذرة التي حدث لها اختزال هي :
الاجابات
Cr
C
H
O
سؤال رقم 34
عدد تأكسد الهيدروجين يساوي ( -1 ) في المركب :
الاجابات
HBr
HClO
CaH2
H2O
سؤال رقم 35
عدد تأكسد النيتروجين N في المركب N2O3 يساوي :
الاجابات
+6
+3
-2
+4
سؤال رقم 36
أحد التفاعلات التالية ليس تفاعل تأكسد واختزال ذاتي :
الاجابات
2H2O2 → 2H2O + O2
Pb + PbO2 + H2SO4 → PbSO4
-Cl2 → OCl- + Cl
-3BrO- → 2Br- + BrO3
سؤال رقم 37
عدد تأكسد البروم يساوي ( +5 ) في المركب :
الاجابات
HBr
HBrO
HBrO4
HBrO3
سؤال رقم 38
عند تأكسد H2S لإنتاج H2SO4 فإن مقدار التغير في عدد تأكسد الكبيريت S هو :
الاجابات
2
6
4
8
سؤال رقم 39
في التفاعل : -HClO → ClO3 التغير في عدد تأكسد الكلور يساوي :
الاجابات
5
4
6
3
سؤال رقم 40
العامل المؤكسد هو المادة التي :
الاجابات
تفقد الالكترونات أثناء التفاعل
يحدث لها تأكسد
تسبب أكسدة مادة أخرى
تسبب اختزال مادة أخرى
سؤال رقم 41
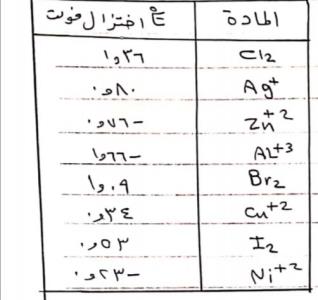

بالاعتماد على الجدول المرفق فإن أقوى عامل محتزل هو:
الاجابات
AL
Ag
Cl-
Br-
سؤال رقم 42
مفاهيم برونستد -لوري فسرت تفاعلات الحموض والقواعد التي لا يحدث فيها انتقال للبروتون بين المواد المتفاعلة
الاجابات
نعم
لا
سؤال رقم 43
ما قيمة الرقم الهيدروجيني pH المتوقعة لمحلول حمضي التأثير :
الاجابات
أقل من 7
تساوي 7
أكبر من 7
تساوي 14
سؤال رقم 44
الرقم الهيدروجيني لمحلول القاعدة KOH تركيزها 1× 10-5 هو :
الاجابات
5
9
6
8
سؤال رقم 45
الرقم الهيدروجيني لمحلول الحمض HCIO4 تركيزه 1×10-4 مول / لتر هو:
الاجابات
4
6
3
10
سؤال رقم 46
الرقم الهيدروجيني لخليط مكون من الحمض الضعيف HA الذي له Ka تساوي 2×10 -5 وملحه KC لهما التركيز نفسه
الاجابات
5
اكبر من 5
أقل من 5
7
سؤال رقم 47
الرقم الهيدروجيني لمحلول HNO3 الذي تركيزه 1 مول/لتر يساوي :
الاجابات
صفر
1
2
3
سؤال رقم 48
العبارة الصحيحة المتعلقة بقيمة الرقم الهيدروجيني هي
الاجابات
تزداد بزيادة حموضة المحلول
تزداد بزيادة قاعدية المحلول
تقل بنقصان +H3O في المحلول
تقل بزيادة - OH في المحلول
سؤال رقم 49
في محلول مائي ل N2H4 تركيزه(0.01) مول/لتر . اذا كان Kb له(610x1-) فإن قيمة الرقم الهيدروجيني للمحلول هي :
الاجابات
6
10
8
12
سؤال رقم 50
المادة التي تستقبل زوج أو أكثر من الالكترونات غير الرابطة هي:
الاجابات
قاعدة لويس
حمض ارهينوس
حمض لويس
حمض برونستد- لوري
سؤال رقم 51
في الماء النقي يكون :
الاجابات
5=PH
-7 10×1 < H3O+
مول / لتر
]OH-[]= H3O+[
PH أكبر من 9
سؤال رقم 52
عند إضافة بلورات الملح CH3COONa إلى محلول الحمض CH3COON فإنه:
الاجابات
تقل PH
OH- يقل
H3O+ يزداد
تزداد PH
سؤال رقم 53
عند اضافة بلورات الملح N2H5CL الى محلول القاعدة N2H4 فإنه:
الاجابات
تزداد PH
H3O+ يقل
OH- يقل
تبقى PH ثابتة
سؤال رقم 54
احدى المواد التالية تعتبر من حموض ( برونستد - لوري) :
الاجابات
Zn+2
SO2
BF3
HCO2H
سؤال رقم 55
احدى المواد التالية ليست من قواعد لويس:
الاجابات
CH3NH2
Br-
SO4-2
Ag+
سؤال رقم 56
القاعدة المرافقة لـ H2SO3
الاجابات
HSO3+
HSO3-
H2SO3+
HSO3
سؤال رقم 57
الحمض المرافق لـ -HCO3 هو :
الاجابات
H2CO3-
CO3-2
H2CO3
HCO3+
سؤال رقم 58
تعد إحدى المواد التالية مادة مترددة ( امفوتيرية) :
الاجابات
HCOO-
NH4+
HCO3-
N-3
سؤال رقم 59
إحدى المحاليل التالية لا يمثل زوج مترافق من الحمض والقاعدة
الاجابات
H2S/ HS-
NH4+/ NH3
HCN/ CN-
H2PO4-/ PO4-3
سؤال رقم 60
الملح الذي لا يتميه من بين التالية هو :
الاجابات
kNO2
NaOCl
LiBr
NH4I
سؤال رقم 61
كتلة حمض البنزويك C6H5COOH اللازم إذابتها في 500 مل من الماء للحصول على محلول له PH تساوي 3 .
ك.م لـلحمض تساوي 122 غ/مول و قيمة Ka له تساوي 1×10 -5
الاجابات
12,2 غ
61 غ
6,1 غ
1,22 غ
سؤال رقم 62
الجدول لعدد من القواعد متساوية التركيز
( 0.1 مول/لتر ) ومعلوات عن كل منها , القاعدة التي لمحلولها أقل تركيز أيونات [ +H3O ] هي :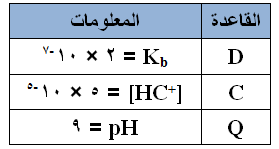

الاجابات
القاعدة C
القاعدة Q
القاعدة D
+DH
سؤال رقم 87
الغاز الناتج من تفاعلCH3OH مع Na هو :
الاجابات
CO2
H2
N2
O2
سؤال رقم 88
اي انواع المركبات الآتية يكشف عنه بمحلول تولنز:
الاجابات
هاليد الايكيل
الكحولات
الكيتونات
الالدهايدات
سؤال رقم 89
تفاعل يتم بين مادتين لانتاج مادة واحدة باستخدام جميع الذرات من المادتين هو تفاعل :
الاجابات
حذف
استبدال
استرة
اضافة
سؤال رقم 90
ادرس المخطط التالي ثم اجب عن الاسئلة التي تليه :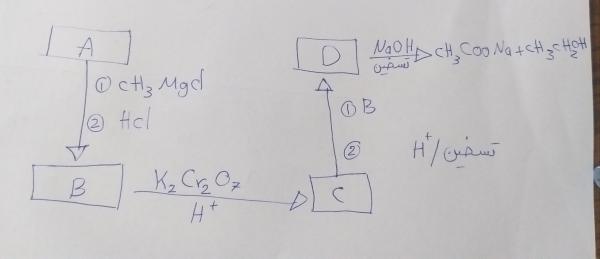

صيغة المركب A هي :
الاجابات
O
||
CH3C-H
CH3OH
HCHO
CH3Br
سؤال رقم 91
صيغة المركب B هي :
الاجابات
CH3CH2OH
CH3COOH
CH3OH
CH3CH2CL
سؤال رقم 92
صيغة المركب C هي :
الاجابات
O
||
CH3C-H
O
||
CH3C-OH
CH3CH2Br
CH3CH2OH
سؤال رقم 93
صيغة المركب D هي :
الاجابات
CH3CH2CH2CH2OH
CH3COOCH2CH3
CH3COOCH3
CH3CH2OCH2CH3
سؤال رقم 94
المركب الذي يتفاعل مع محلول تولنز ويكون مرآة فضيةهو :
الاجابات
CH3CH2OH
CH3CHO
CH3COOH
CH3CH2Br
سؤال رقم 95
صيغة المركب الناتج من تفاعل التالي 

الاجابات
OH
|
CH3CHCH3
CH3CH2CH2OH
CH3CH2COOH
CH3CH=CH2
سؤال رقم 96
في التفاعل التالي فإن قيمة x تمثل :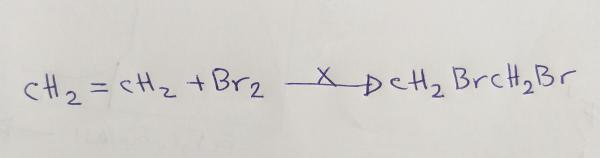
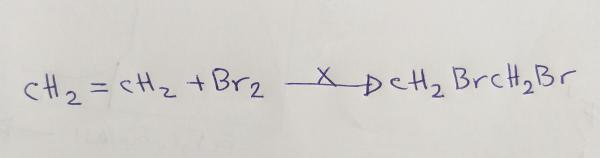
الاجابات
CCL4
H2
HBr
ضوء
سؤال رقم 97
في التفاعل التالي فإن قيمة xتمثل :

الاجابات
CCL4
H2
HBr
ضوء
سؤال رقم 98
المركب الناتج من تفاعل CH3ONa مع CH3CL
الاجابات
CH3CH2CL
CH3OCH3
CH3CH2OH
O
‖
CH3C-H
سؤال رقم 99
يتم الحصول CH3CBr2CH3 من تفاعل ٢ مول من HBr مع :
الاجابات
CH ≡CH
CH3CHCH2
CH3C ≡CH
CH3C-CH3
‖
O
سؤال رقم 100
التفاعل الذي يحدث للالكانات هو :
الاجابات
الحذف
الاضافه
التأكسد
الاستبدال (الهلجنه)
سؤال رقم 101
الكحول الذي شارك في تكوين الاستر الاتي هو 

الاجابات
CH3OH
CH3CH2OH
OH
|
CH3CHCH3
CH3CH2CH2OH
سؤال رقم 102
المركب الذي لا يتأكسد لمحلول دايكرومات البوتاسيوم الحمضي +K2cr2o7/H
هو
الاجابات
CH3CH2CHO
CH3CH2CH2OH
CH3CHOHCH3
CH3)3 COH
سؤال رقم 103
تصدأ برادة الحديد بشكل اسرع من سلك حديد لهما نفس الكتلة عند نفس الظروف الجوية فإن العامل المؤثر في سرعة التفاعل هو :
الاجابات
درجة الحرارة
مساحة السطح
طبيعة المادة
التركيز
سؤال رقم 104
اذا كانت قيمة ثابت السرعة K =٢×١٠_٤لتر٢/مول٢. ث
فإن الرتبة الكلية للتفاعل هي
الاجابات
١
٢
٣
٤
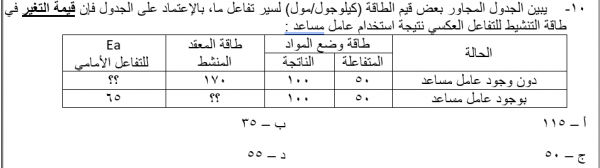
سؤال رقم 105


الاجابات
٤×١٠-٧
٤×١٠-٦
٨×١٠-٤
٢×١٠_٦
سؤال رقم 106
قانون سرعة التفاعل يمثل العلاقة بين :
الاجابات
درجة الحرارة والتركيز
سرعة التفاعل ودرجة الحرارة
سرعة التفاعل والزمن
سرعة التفاعل والتركيز
سؤال رقم 107
يكون تركيز المواد المتفاعلة في التفاعل
A+B-----> C+D
(A)و(B) اعلى عند الزمن
الاجابات
٢ث
٤ ث
٦ث
١٠ ث
سؤال رقم 108
سرعة التفاعل عند الزمن صفر لحظة خلط المواد المتفاعله تمثل :
الاجابات
السرعه اللحظية
السرعة الابتدائية
معدل سرعة التفاعل
السرعة النهائية
سؤال رقم 118
الجدول لعدد من القواعد متساوية التركيز
( 0.1 مول/لتر ) ومعلوات عن كل منها , القاعدة التي لمحلولها أقل تركيز أيونات [ +H3O ] هي :

الاجابات
القاعدة C
القاعدة Q
القاعدة D
+DH
سؤال رقم 119
في المركب -3[Fe(CN)6]حمض لويس هو Fe+3
الاجابات
نعم
لا
سؤال رقم 120
في الجدول التالي والذي يمثل مجموعة حموض متساوية التركيز [ 0,1 ] مول/لتر وقيم Ka لكل منها , صيغة القاعدة المرافقة الأقوى هي :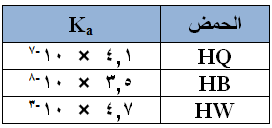

الاجابات
-W
-B
W
-Q
سؤال رقم 121
قيمة PH لمحلول القاعدة LiOH تركيزه يساوي 1×10 -4 تساوي 4
الاجابات
نعم
لا
سؤال رقم 122
الجدول لعدد من القواعد وقيم Kb لكل منها , صيغة أقوى حمض مرافق :


الاجابات
+N2H5
+NH4
+CH3NH3
+C2H5NH3
سؤال رقم 123
فسر العالم أرهينيوس السلوك الحمضي لملح NH4I
الاجابات
نعم
لا
سؤال رقم 124
حموض لويس هي مواد مانحة لزوج أو أكثر من الالكترونات
الاجابات
نعم
لا
سؤال رقم 125
القاعدة B لها PH تساوي 10 والقاعدة D لها PH تساوي 12, فإن تركيز أيونات [+H3O] في محلول القاعدة B أعلى منه في محلول القاعدة D
الاجابات
نعم
لا
سؤال رقم 126
ما أثر إضافة الملح KNO2 إلى محلول HNO2 ؟
الاجابات
زيادة [+H3O]
نقص [+H3O]
نقص قيمة PH
نقص [HNO2]
سؤال رقم 127
المحلول الذي له أعلى PH من بين المحاليل الآتية المتساوية في التركيز هو :
الاجابات
KBr
NaNO2
N2H5NO3
KOH
سؤال رقم 128
المادة التي تمثل حمض لويس فقط فيما يلي هي :
الاجابات
-Cl
NF3
2+Cu
H2O
سؤال رقم 129
صيغة الحمض المرافق الناتج من تفاعل NH2OH و H2O هي :
الاجابات
+H3O
H2O
+NH3OH
+NH2OH
سؤال رقم 133
الحمض في الأيون -3[Co(CN)6] هو :
الاجابات
-CN
3-Co
3+CN
3+Co
سؤال رقم 134
أي الآتي فشل أرهينيوس في تفسير سلوكه الحمضي أو القاعدي:
الاجابات
HF
+NH4
NaNO2
-OH
سؤال رقم 138
الملح الذي لا يتميه من بين التالية هو :
الاجابات
KF
NaCN
LiBr
NH4NO3
سؤال رقم 139
إضافة ملح KHS إلى محلول حمض H2S يزيد من تركيز أيونات [-OH]
الاجابات
نعم
لا
سؤال رقم 149
عند اضافة 0,04 مول منNaNO2 الى لتر من محلول الحمض HNO2 الذي تركيزه (0,1) مول/لتر وكانت قيمة Ka للحمض = 4*10-4 فان قيمة PH للمحلول هي
الاجابات
3
4
6
1
سؤال رقم 150
الايون المشترك في المحلول المكون من الحمض HCOOH والملح HCOONa هو
الاجابات
-COONa
-HCOO
+HCOO
+COOH3
سؤال رقم 151
محلول مائي لقاعدة ضعيفة B تركيزه ( 0.01 ) مول/لتر وكان Kb لها تساوي 1,6*10-9 و Kw = 1*10-14 فان تركيز +H3O في المحلول هو
الاجابات
4*10-5
4*10-6
2,5*10-9
2,5*10-10
سؤال رقم 152
اي الأملاح الآتية يعد ذوبانها في الماء تميه
الاجابات
LiCl
KI
KF
NaClO4
سؤال رقم 153
المحلول الذي تكون قاعدته المرافقه هي الأضعف

الاجابات
HA
HB
HC
HD
سؤال رقم 154
العبارة الصحيحة المتعلقة بقيمة الرقم الهيدروجيني هي
الاجابات
تزداد بزيادة حموضة المحلول
تزداد بزيادة قاعدية المحلول
تقل بنقصان +H3O في المحلول
تقل بزيادة - OH في المحلول
سؤال رقم 155
يصنف محلول HClO4 بأنه محلول
الاجابات
حمض قوي
حمض ضعيف
قاعدة قوية
قاعدة ضعيفة
سؤال رقم 156
احد المحاليل الآتية المتساوية في التركيز يكون فيه [-OH] هو الأقل
الاجابات
NaOH
KOH
HNO3
NH3
سؤال رقم 157
احد المحاليل الآتية المتساوية في التركيز يكون فيه [-OH] هو الأقل
الاجابات
NaOH
KOH
HNO3
NH3
سؤال رقم 158
مادة تسلك سلوكا امفوتيريا
الاجابات
-HSO3
+H3O
CH3NH2
-HCOO
امتحانات مشابهه لأمتحان الكيمياء
1- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 6032-5
عدد مقدمي الامتحان 1811
عدد مقدمي الامتحان 1811
2- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 2074-11
عدد مقدمي الامتحان 308
عدد مقدمي الامتحان 308
3- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 15136-3
عدد مقدمي الامتحان 306
عدد مقدمي الامتحان 306
4- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 2228-6
عدد مقدمي الامتحان 191
عدد مقدمي الامتحان 191
5- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 1114-33
عدد مقدمي الامتحان 136
عدد مقدمي الامتحان 136
6- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 2228-1
عدد مقدمي الامتحان 99
عدد مقدمي الامتحان 99
7- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 3797-35
عدد مقدمي الامتحان 80
عدد مقدمي الامتحان 80
8- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 1490-13
عدد مقدمي الامتحان 79
عدد مقدمي الامتحان 79
9- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 15136-4
عدد مقدمي الامتحان 78
عدد مقدمي الامتحان 78
10- امتحان الكيمياء الصف الثاني ثانوي الفصل مراجعة - 11566-4
عدد مقدمي الامتحان 78
عدد مقدمي الامتحان 78
امتحانات اخرى للصف الثاني ثانوي
1- امتحان الحاسوب الصف الثاني ثانوي الفصل الأول - 2742-11
عدد مقدمي الامتحان 3564
عدد مقدمي الامتحان 3564
2- امتحان التاريخ الصف الثاني ثانوي الفصل الأول - 5448-6
عدد مقدمي الامتحان 2751
عدد مقدمي الامتحان 2751
3- امتحان اللغة العربية الصف الثاني ثانوي الفصل الأول - 5229-4
عدد مقدمي الامتحان 2349
عدد مقدمي الامتحان 2349
4- امتحان اللغة العربية الصف الثاني ثانوي الفصل الثاني - 1502-1
عدد مقدمي الامتحان 2011
عدد مقدمي الامتحان 2011
5- امتحان الحاسوب الصف الثاني ثانوي الفصل الثاني - 879-6
عدد مقدمي الامتحان 1912
عدد مقدمي الامتحان 1912
6- امتحان التربية الاسلامية الصف الثاني ثانوي الفصل الأول - 4388-4
عدد مقدمي الامتحان 1853
عدد مقدمي الامتحان 1853
7- امتحان الكيمياء الصف الثاني ثانوي الفصل الأول - 6032-5
عدد مقدمي الامتحان 1811
عدد مقدمي الامتحان 1811
8- امتحان التربية الاسلامية الصف الثاني ثانوي الفصل الثاني - 1965-1
عدد مقدمي الامتحان 1387
عدد مقدمي الامتحان 1387
9- امتحان اللغة العربية الصف الثاني ثانوي الفصل الأول - 1370-9
عدد مقدمي الامتحان 1323
عدد مقدمي الامتحان 1323
10- امتحان الحاسوب الصف الثاني ثانوي الفصل الأول - 2742-13
عدد مقدمي الامتحان 1301
عدد مقدمي الامتحان 1301