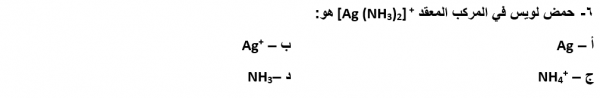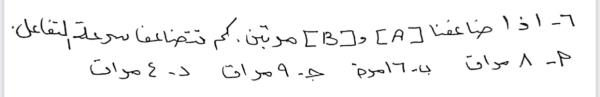امتحان الكيمياء للصف الثاني ثانوي | نماذج وأسئلة الفصل الثاني 2025
يعد امتحان الكيمياء للصف الثاني ثانوي من أهم الامتحانات التي يتطلع الطلاب للنجاح فيها خلال الفصل الثاني. نقدم لك في هذا المقال نماذج امتحانية محدثة وأسئلة متوقعة لتساعدك في التحضير بشكل فعّال، مع نصائح مهمة لاستكمال الاستعداد للامتحان بثقة. تابع القراءة لاكتشاف المزيد حول الأسئلة الأكثر شيوعاً وكيفية التفوق في امتحانك.
سؤال رقم 1
مقدار التغير في عدد تأكسد cr في التفاعل هو :
الاجابات
6
4
3
2
سؤال رقم 2
عدد تأكسد CL = +1 في المركب
الاجابات
HClO3
HClO
HClO4
HCl
سؤال رقم 3
: هو Mn فإن مقدار التغير في عدد تأكسد Mn+2 وتحولها إلى MnO4- عند اختزال
الاجابات
7
2
3
5
سؤال رقم 4
التفاعل الذي يحتاج إلى عامل مؤكسد هو :
الاجابات
N2O4 →NO
NO → N2
Ti+3 → TiO+2
NO2 → N2O4
سؤال رقم 5
أي المواد التالية يمكن أن يسلك كعامل مؤكسد
الاجابات
K+
Cl-
O-2
Na
سؤال رقم 6
أي المواد التالية يمكن أن يسلك كعامل مختزل
الاجابات
Na+
Br-
Br2
O2
سؤال رقم 7
إذا كانت قيمة PH
لمحلول الحمض HF = 7.2 وتركيز الحمض HF = 01.0 مول/ لتر ( لو 2= 3.0) فإن قيمة Ka هي:
الاجابات
4× 10
4 ×10 -4
2 ×10 -4
2 ×10 -6
سؤال رقم 8
في الماء النقي يكون :
الاجابات
5=PH
-7 10×1 < H3O+
مول / لتر
]OH-[]= H3O+[
PH أكبر من 9
سؤال رقم 9
الرقم الهيدروجيني لمحلول القاعدة KOH تركيزها 1× 10-5 هو :
الاجابات
5
9
6
8
سؤال رقم 10
احدى المواد التالية تعتبر من حموض ( برونستد - لوري) :
الاجابات
Zn+2
SO2
BF3
HCO2H
سؤال رقم 11
احدى المواد التالية ليست من قواعد لويس:
الاجابات
CH3NH2
Br-
SO4-2
Ag+
سؤال رقم 12
القاعدة المرافقة لـ H2SO3
الاجابات
HSO3+
HSO3-
H2SO3+
HSO3
سؤال رقم 13
تعد إحدى المواد التالية مادة مترددة ( امفوتيرية) :
الاجابات
HCOO-
NH4+
HCO3-
N-3
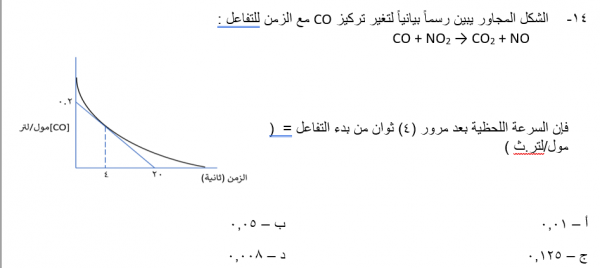
سؤال رقم 14
احدى المواد التالية عجز ارهينوس عن تفسير سلوكها القاعدي:
الاجابات
HBr
KCN
NaOH
NH4C1
سؤال رقم 15
إحدى المحاليل التالية لا يمثل زوج مترافق من الحمض والقاعدة
الاجابات
H2S/ HS-
NH4+/ NH3
HCN/ CN-
H2PO4-/ PO4-3
سؤال رقم 16
الحمض المرافق لــ 2- HPO4 هو
الاجابات
3- PO4
H2PO4
-H2PO4
- PO4
سؤال رقم 17
حموض لويس هي مواد مانحة لزوج أو أكثر من الالكترونات
الاجابات
نعم
لا
سؤال رقم 18
قيمة PH تساوي 2 في محلول :
الاجابات
0,01 مول/لتر HF
0,01 مول/لتر HI
0,01 مول/لتر HCN
0,01 مول/لتر HOCl
سؤال رقم 19
كتلة حمض البنزويك C6H5COOH اللازم إذابتها في 500 مل من الماء للحصول على محلول له PH تساوي 3 .
ك.م لـلحمض تساوي 122 غ/مول و قيمة Ka له تساوي 1×10 -5
الاجابات
12,2 غ
61 غ
6,1 غ
1,22 غ
سؤال رقم 20
عدد مولات ملح CH3COONa التي يجب إذابتها في لتر واحد من محلول حمض الايثانويك CH3COOH الذي تركيزه 0,1 مول/لتر للحصول على محلول له PH تساوي 5 . ( Ka للحمض تساوي 2×10 -5 )
الاجابات
0,25 مول
2 مول
0,2 مول
4 مول
سؤال رقم 21
الجدول لعدد من القواعد متساوية التركيز
( 0.1 مول/لتر ) ومعلوات عن كل منها , القاعدة التي لمحلولها أقل تركيز أيونات [ +H3O ] هي :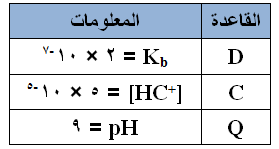

الاجابات
القاعدة C
القاعدة Q
القاعدة D
+DH
سؤال رقم 22
في المركب -3[Fe(CN)6]حمض لويس هو Fe+3
الاجابات
نعم
لا
سؤال رقم 23
في الجدول التالي والذي يمثل مجموعة حموض متساوية التركيز [ 0,1 ] مول/لتر وقيم Ka لكل منها , صيغة القاعدة المرافقة الأقوى هي :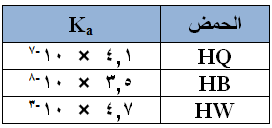

الاجابات
-W
-B
W
-Q
سؤال رقم 24
الجدول لعدد من القواعد وقيم Kb لكل منها , صيغة أقوى حمض مرافق :


الاجابات
+N2H5
+NH4
+CH3NH3
+C2H5NH3
سؤال رقم 25
قيمة PH لمحلول القاعدة LiOH تركيزه يساوي 1×10 -4 تساوي 4
الاجابات
نعم
لا
سؤال رقم 26
المادة التي تسلك كقاعدة فقط وفق مفاهيم برونستد-لوري هي :
الاجابات
-HS
CH3COOH
-HCO3
-HCO2
سؤال رقم 27
فسر العالم أرهينيوس السلوك الحمضي لملح NH4I
الاجابات
نعم
لا
سؤال رقم 28
المادة التي تعد قاعدة أرهينيوس من بين التالية هي :
الاجابات
NH3
KF
LiOH
HCN
سؤال رقم 29
المادة التي تمثل حمض لويس فقط فيما يلي هي :
الاجابات
-Cl
NF3
2+Cu
H2O
سؤال رقم 30
صيغة الحمض المرافق الناتج من تفاعل NH2OH و H2O هي :
الاجابات
+H3O
H2O
+NH3OH
+NH2OH
سؤال رقم 33
أحد الأزواج الآتية هو زوج مترافق من تفاعل NH3 و -HCO3
الاجابات
HCO3-/H2CO3
HCO3-/NH3
2-HCO3-/CO3
+HCO3-/NH4
سؤال رقم 35
الحمض في الأيون -3[Co(CN)6] هو :
الاجابات
-CN
3-Co
3+CN
3+Co
سؤال رقم 38
أي الآتي فشل أرهينيوس في تفسير سلوكه الحمضي أو القاعدي:
الاجابات
HF
+NH4
NaNO2
-OH
سؤال رقم 41
المادة المترددة من بين المواد الآتية, هي :
الاجابات
-HCOO
+CH3NH3
-CH3CO2
-HCO3
سؤال رقم 42
المحلول الأكثر قاعدية من بين المحاليل التالية هو المحلول الذي له :
الاجابات
PH تساوي 9
تركيز [+H3O ] يساوي 1×10 -4
تركيز [-OH] يساوي 1×10 -11
تركيز [-OH] يساوي 1×10 -2
سؤال رقم 56
تصدأ برادة الحديد بشكل اسرع من سلك حديد لهما نفس الكتلة عند نفس الظروف الجوية فإن العامل المؤثر في سرعة التفاعل هو :
الاجابات
درجة الحرارة
مساحة السطح
طبيعة المادة
التركيز
سؤال رقم 57
قانون سرعة التفاعل يمثل العلاقة بين :
الاجابات
درجة الحرارة والتركيز
سرعة التفاعل ودرجة الحرارة
سرعة التفاعل والزمن
سرعة التفاعل والتركيز
سؤال رقم 58
اعلى قيمة لطاقة الوضع في منحنى سير التفاعل الكيميائي تكون ل:
الاجابات
المعقد المنشط
المواد الناتجه
المواد المتفاعلة
طاقة التنشيط
سؤال رقم 59
تزداد سرعة التفاعل عند رفع درجة الحرارة بسبب :
الاجابات
نقصان ثابت سرعة التفاعل
زيادة طاقة المعقد المنشط
زيادة عدد التصادمات الفعالة
نقصان طاقة التنشيط
سؤال رقم 60
سرعة التفاعل عند الزمن صفر لحظة خلط المواد المتفاعله تمثل :
الاجابات
السرعه اللحظية
السرعة الابتدائية
معدل سرعة التفاعل
السرعة النهائية
سؤال رقم 77
مركب يتكون من 3 حلقات سداسية وواحدة خماسية بالاضافة الى سلسلة هيدروكربونية ,فإنه ينتمي الى :
الاجابات
البروتينات
الستيرويدات
الدهون
الكربوهيدرات
سؤال رقم 78
يمثل سكر احادي كيتوني خماسي الحلقة , هو:
الاجابات
الغلوكوز
المالتوز
الاميلوز
الفركتوز
سؤال رقم 79
يتكون من وحدتين اساسيتين مرتبطتين برابطة غلايكوسيدية من نوع (الفا , بيتا -1:2) , هو:
الاجابات
السكروز
الاميلوز
الفركتوز
المالتوز
سؤال رقم 80
يشكل دعامه لهيكل النبات , هو:
الاجابات
الاميلوبكتين
الاميلوز
السليلوز
الفركتوز
سؤال رقم 81
يتفاعل مع الحموض الدهنية مكونا ثلاثي غليسرايد, هو:
الاجابات
الغلوكوز
الغليسرول
السليلوز
البروتين
سؤال رقم 82
يوجد على شكل سلاسل غير متفرعة وترتبط وحداته الاساسية بالرابطة الغلايكوسيدية (الفا- 1:4) , هو:
الاجابات
السكروز
الفركتوز
الغلايكوجين
الأميلوز
سؤال رقم 83
يوجد في المحلول المائي على شكل أيون مزدوج, هو:
الاجابات
السليلوز
الحمض الاميني
الدهون
النشا
سؤال رقم 84
مركب يتحلل في الوسط الحمضي منتجا غليسرول و3 حموض دهنية ,هو:
الاجابات
ثلاثي غليسرايد
الغلوكوز
البروتين
الستيرويدات
سؤال رقم 85
جزء من سلسلة بروتين مكون من خمسة حموض أمينية , عدد الروابط الببتيدية فيها تساوي:
الاجابات
5
3
4
2
سؤال رقم 86
جزء من سلسلة بروتين مكون من خمسة حموض أمينية , عدد الروابط الببتيدية فيها تساوي:
الاجابات
5
3
4
2
سؤال رقم 87
أحد المركبات التالية زيادة نسبته في الدم تسبب تصلب في الاوعية الدموية
الاجابات
المالتوز
الكوليسترول
الغليسرول
الفركتوز
سؤال رقم 89
قيمة PH لمحلول حضر بإذابة 8 غم من NaOH في الماء للحصول على محلول حجمه 400 مل هي :
( ك.م لـــ NaOH تساوي 40 غ/مول ) / لو 2 = 0,3
الاجابات
13,7
12,3
11
13,3
سؤال رقم 90
المادة التي تعد قاعدة أرهينيوس من بين التالية هي :
الاجابات
NH3
KF
LiOH
HCN
سؤال رقم 91
محلول قاعدة ضعيفة تركيزه ٠,١ مول /لتر و قيمة ph له =٩ فإن قيمة Kb للقاعدة تساوي
الاجابات
1X10-4
1X10-8
1X10-9
1X10-10
سؤال رقم 92
عند اختزال ايون - MnO4 إلى MnO2 فإن التغير في عدد التأكسد ل Mn هو
الاجابات
٣
٤
٥
٧
سؤال رقم 93
أعلى عدد تأكسد للنتروجين يكون في
الاجابات
-NO3
N2O3
N2O4
NO
سؤال رقم 94
الرقم الهيدروجيني لمحلول HBr تركيزه 3X10-2 مول /لتر اذا علمت ان لو3=0.5
الاجابات
3
2.5
2
1.5
سؤال رقم 95
محلول HI تركيزه 1X10-2 مول /لتر فإن تركيز ايون - OH مول /لتر هو
الاجابات
1X10-2
1X10-14
1X10-12
2X10-2
سؤال رقم 96
نوع الرابطة المتكونة عند تفاعل NH3 و أيون +H لتكوين +NH4 هي رابطة
الاجابات
تساهمية
ايونية
هيدروجينية
تناسقية
سؤال رقم 97
يصنف محلول HClO4 بأنه محلول
الاجابات
حمض قوي
حمض ضعيف
قاعدة قوية
قاعدة ضعيفة
سؤال رقم 98
اذا كان لديك محلول قيمة PH له =10.8 فإن طبيعة هذا المحلول :
الاجابات
متعادل
حمضي
قاعدي
سؤال رقم 99
اعتمادا علىى الجدول المجاور لمحاليل حموض ضعيفة متساوية التركيز أجيبي عن الاسئله التي تليه: من(س4 الى س8)
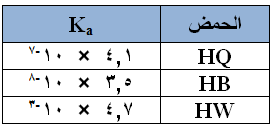

صيغة الحمض الاضعف هي:
الاجابات
HW
HB
HQ
سؤال رقم 100
صيغة القاعدة المرافقة الاضعف هي:
الاجابات
-W
-Q
-B
سؤال رقم 101
الحمض الذي لديه اكبر قدرة للتأين في الماء هو :
الاجابات
HQ
HB
HW
سؤال رقم 108
ان قيمة PH لمحلول KOH تركيزه 0.01 مول / لتر تساوي :
الاجابات
2
12
10
1
سؤال رقم 109
العبارة الصحيحة المتعلقة بقيمة الرقم الهيدروجيني هي
الاجابات
تزداد بزيادة حموضة المحلول
تزداد بزيادة قاعدية المحلول
تقل بنقصان +H3O في المحلول
تقل بزيادة - OH في المحلول
سؤال رقم 111
سرعة التفاعل عند الزمن صفر لحظة خلط المواد المتفاعله تمثل :
الاجابات
السرعه اللحظية
السرعة الابتدائية
معدل سرعة التفاعل
السرعة النهائية
سؤال رقم 112
يكون تركيز المواد المتفاعلة في التفاعل
A+B-----> C+D
(A)و(B) اعلى عند الزمن
الاجابات
٢ث
٤ ث
٦ث
١٠ ث
سؤال رقم 113
اذا كانت قيمة ثابت السرعة K =٢×١٠_٤لتر٢/مول٢. ث
فإن الرتبة الكلية للتفاعل هي
الاجابات
١
٢
٣
٤
سؤال رقم 114
تصدأ برادة الحديد بشكل اسرع من سلك حديد لهما نفس الكتلة عند نفس الظروف الجوية فإن العامل المؤثر في سرعة التفاعل هو :
الاجابات
درجة الحرارة
مساحة السطح
طبيعة المادة
التركيز
سؤال رقم 116
الجدول لعدد من القواعد متساوية التركيز
( 0.1 مول/لتر ) ومعلوات عن كل منها , القاعدة التي لمحلولها أقل تركيز أيونات [ +H3O ] هي :

الاجابات
القاعدة C
القاعدة Q
القاعدة D
+DH
سؤال رقم 117
الحمض المرافق لـ -HCO3 هو :
الاجابات
H2CO3-
CO3-2
H2CO3
HCO3+
سؤال رقم 118
القاعدة المرافقة لـ H2SO3
الاجابات
HSO3+
HSO3-
H2SO3+
HSO3
سؤال رقم 119
احدى المواد التالية ليست من قواعد لويس:
الاجابات
CH3NH2
Br-
SO4-2
Ag+
سؤال رقم 120
احدى المواد التالية تعتبر من حموض ( برونستد - لوري) :
الاجابات
Zn+2
SO2
BF3
HCO2H
سؤال رقم 121
المادة التي تستقبل زوج أو أكثر من الالكترونات غير الرابطة هي:
الاجابات
قاعدة لويس
حمض ارهينوس
حمض لويس
حمض برونستد- لوري
سؤال رقم 122
في محلول مائي ل N2H4 تركيزه(0.01) مول/لتر . اذا كان Kb له(610x1-) فإن قيمة الرقم الهيدروجيني للمحلول هي :
الاجابات
6
10
8
12
سؤال رقم 123
ما قيمة الرقم الهيدروجيني pH المتوقعة لمحلول حمضي التأثير :
الاجابات
أقل من 7
تساوي 7
أكبر من 7
تساوي 14
سؤال رقم 124
في التفاعل : -HClO → ClO3 التغير في عدد تأكسد الكلور يساوي :
الاجابات
5
4
6
3
سؤال رقم 125
عند تأكسد H2S لإنتاج H2SO4 فإن مقدار التغير في عدد تأكسد الكبيريت S هو :
الاجابات
2
6
4
8
سؤال رقم 126
عدد تأكسد البروم يساوي ( +5 ) في المركب :
الاجابات
HBr
HBrO
HBrO4
HBrO3
سؤال رقم 127
العامل المؤكسد هو المادة التي :
الاجابات
تفقد الالكترونات أثناء التفاعل
يحدث لها تأكسد
تسبب أكسدة مادة أخرى
تسبب اختزال مادة أخرى
سؤال رقم 128
في التفاعل :
Cr2O7-2 + C2H6O → Cr+3 + C2H4O
الذرة التي حدث لها اختزال هي :
الاجابات
Cr
C
H
O
سؤال رقم 129
في التفاعل :
Cr2O7-2 + C2H6 O → Cr+3 + CO2
والذي يحدث في وسط حمضي . فإن المعادلة التي تمثل نصف تفاعل الاختزال الموزون هي :
الاجابات
-C2H6O + 3H2O → 2CO2 + 6H+ + 6e
-C2H6O + 3H2O → 2CO2 + 12H+ +12e
Cr2O7-2 + 14H+ + 6e- → 2Cr+3 + 7H2O
-Cr2O7-2 + 3H2O → 2Cr+3 +10H+ + 14e
سؤال رقم 130
إذا علمت أن التفاعل التالي ممكن الحدوث في الظروف المعيارية :
-Br2 + Ni → Ni+2 + 2Br فإن العبارة الصحيحة فيما يلي هي :
الاجابات
Br2 عامل مختزل
Ni هو المهبط
-Br عامل مختزل أقوى من الــ Ni
Br2 عامل مؤكسد أقوى من الــ Ni+2
سؤال رقم 131

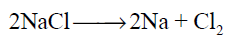
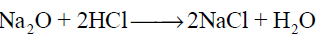
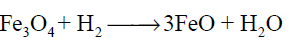
أحد التفاعلات التالية لا يعد تفاعل تأكسد واختزال :
الاجابات

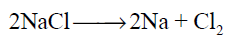
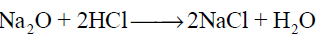
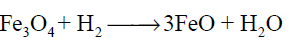
سؤال رقم 132
المعادلة النهائية الموزونة للتفاعل التالي والذي يحدث في وسط حمضي هي :
H2S + NO3- → S + NO
الاجابات
2H2S + 3NO3- → 2S + 3NO + 2H2O
3H2S + 2NO3- + 2H+ → 3S + 2NO + 4H2O
3H2S + 2NO3- + 2H2O → 3S + 2NO
3H2S + 2NO3- → 3S + 2NO + H2O
سؤال رقم 133
لدى موازنة التفاعل التالي في وسط قاعدي :
CN- + MnO4- → CNO- + MnO2
فإن عدد مولات الالكترونات المفقودة أو المكتسبة في التفاعل يساوي:
الاجابات
2
4
6
3
سؤال رقم 134
العامل المختزل هو المادة التي تسبب أكسدة مادة أخرى
الاجابات
نعم
لا
سؤال رقم 135
نصف التفاعل Cr+3 + 3e- → Cr يحتاج إلى عامل مؤكسد
الاجابات
نعم
لا
سؤال رقم 136
في التفاعل :
Al + NO3- → AlO2- + NH3
العامل المؤكسد هو -NO3
الاجابات
نعم
لا
سؤال رقم 137
في التحول -HBrO → BrO3 مقدار التغير في عدد تأكسد البروم يساوي 6
الاجابات
نعم
لا
سؤال رقم 138
عدد تأكسد الكربون في سكر الغلوغوز C6H12O6 يساوي +4
الاجابات
نعم
لا
سؤال رقم 139
يعرف عدد التأكسد بأنه الشحنة الفعلية لأيون الذرة في المركبات الأيونية
الاجابات
نعم
لا
سؤال رقم 140
يعتبر هذا التفاعل
CH4(s) + 2O2(g) → CO2(g) + 2H2O(g) ∆H = -882kJ ؟
الاجابات
تفاعل ماص للطاقة
تفاعل طارد للطاقة
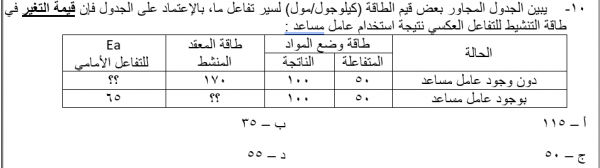
سؤال رقم 141
الشكل المجاور يمثل نفس التفاعل بوجود عامل مساعد وبدون عامل مساعد اختر رمز الاجابة الصحيحة:

الاجابات
طاقة التنشيط بوجود عامل مساعد تمثل X
طاقة التنشيط بدون عامل مساعد تمثل Y
الرسم المجاور يمثل اثر العامل المساعد على قيمة H∆
لا نستطيع من خلال الرسم ان نستدل على وجود العامل المساعد
سؤال رقم 142
اعلى قيمة لطاقة الوضع في منحنى سير التفاعل الكيميائي تكون ل:
الاجابات
المعقد المنشط
المواد الناتجه
المواد المتفاعلة
طاقة التنشيط
امتحانات مشابهه لأمتحان الكيمياء
1- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 6032-5
عدد مقدمي الامتحان 1811
عدد مقدمي الامتحان 1811
2- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 2074-11
عدد مقدمي الامتحان 308
عدد مقدمي الامتحان 308
3- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 15136-3
عدد مقدمي الامتحان 306
عدد مقدمي الامتحان 306
4- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 2228-6
عدد مقدمي الامتحان 191
عدد مقدمي الامتحان 191
5- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 1114-33
عدد مقدمي الامتحان 136
عدد مقدمي الامتحان 136
6- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 2228-1
عدد مقدمي الامتحان 99
عدد مقدمي الامتحان 99
7- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 3797-35
عدد مقدمي الامتحان 80
عدد مقدمي الامتحان 80
8- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 1490-13
عدد مقدمي الامتحان 79
عدد مقدمي الامتحان 79
9- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 15136-4
عدد مقدمي الامتحان 78
عدد مقدمي الامتحان 78
10- امتحان الكيمياء الصف الثاني ثانوي الفصل الثاني - 11566-4
عدد مقدمي الامتحان 78
عدد مقدمي الامتحان 78
امتحانات اخرى للصف الثاني ثانوي
1- امتحان الحاسوب الصف الثاني ثانوي الفصل الأول - 2742-11
عدد مقدمي الامتحان 3564
عدد مقدمي الامتحان 3564
2- امتحان التاريخ الصف الثاني ثانوي الفصل الأول - 5448-6
عدد مقدمي الامتحان 2751
عدد مقدمي الامتحان 2751
3- امتحان اللغة العربية الصف الثاني ثانوي الفصل الأول - 5229-4
عدد مقدمي الامتحان 2349
عدد مقدمي الامتحان 2349
4- امتحان اللغة العربية الصف الثاني ثانوي الفصل الثاني - 1502-1
عدد مقدمي الامتحان 2011
عدد مقدمي الامتحان 2011
5- امتحان الحاسوب الصف الثاني ثانوي الفصل الثاني - 879-6
عدد مقدمي الامتحان 1912
عدد مقدمي الامتحان 1912
6- امتحان التربية الاسلامية الصف الثاني ثانوي الفصل الأول - 4388-4
عدد مقدمي الامتحان 1853
عدد مقدمي الامتحان 1853
7- امتحان الكيمياء الصف الثاني ثانوي الفصل الأول - 6032-5
عدد مقدمي الامتحان 1811
عدد مقدمي الامتحان 1811
8- امتحان التربية الاسلامية الصف الثاني ثانوي الفصل الثاني - 1965-1
عدد مقدمي الامتحان 1387
عدد مقدمي الامتحان 1387
9- امتحان اللغة العربية الصف الثاني ثانوي الفصل الأول - 1370-9
عدد مقدمي الامتحان 1323
عدد مقدمي الامتحان 1323
10- امتحان الحاسوب الصف الثاني ثانوي الفصل الأول - 2742-13
عدد مقدمي الامتحان 1301
عدد مقدمي الامتحان 1301